Fracción molar
La fracción molar no tiene unidades, porque representa la relación que existe entre componentes. Al componente A lo representamos en fracción molar como XA y lo definimos así:
Representación
Se representa con la (XA)
📌 Fórmula:


Un mol es la cantidad de sustancia que contiene 6.022 × 10²³ partículas (átomos, moléculas, iones, etc.). Este número es conocido como el número de Avogadro.
Características
-
No tiene unidades, es un número adimensional (entre 0 y 1).
-
Se expresa con decimales o porcentajes (por ejemplo: 0.3 o 30%).
-
La suma de las fracciones molares de todos los componentes es siempre igual a 1:
-
Es útil en:
-
Cálculos de presión parcial (Ley de Dalton)
-
Propiedades coligativas (descenso de presión de vapor, etc.)
-
Mezclas líquidas o gaseosas
-
-
Es independiente de la temperatura y el volumen, ya que depende solo de la cantidad de moles.

Aprende jugando
¡AQUÍ!



Ejemplo 1: Disolución de agua + etanol
Se mezclan 4 mol de agua (H₂O) y 2 mol de etanol (C₂H₅OH).
Proceso:

Ejemplo 2: Solución de NaCl en agua
Se disuelven 1 mol de NaCl en 9 mol de agua.
Proceso:
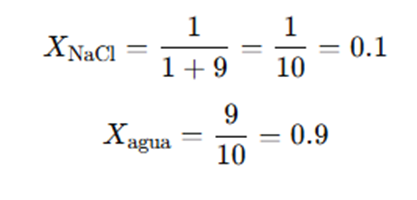
Desafía tus límites con estos ejercicios de química y conviértete en un experto.

